Příprava oxidu měďnatého
CuO : černý prášek (monoklinická prizmatická mřížka), ve vodě téměř nerozpustný, rozpustný v kyselinách.
Reakcí hydroxidu alkalického kovu s roztokem pentahydrátu síranu měďnatého se připraví sraženina hydroxidu měďnatého. Zahřátím se hydroxid měďnatý rozloží za vzniku oxidu měďnatého.
2 NaOH + CuSO4 • 5H2O ?› Cu(OH)2 + Na2SO4 + 5 H2O
Cu(OH)2 ?› CuO + H2O
2 NaOH + CuSO4 • 5H2O ?› Cu(OH)2 + Na2SO4 + 5 H2O
Cu(OH)2 ?› CuO + H2O
Chemikálie a pomůcky:
Pentahydrát síranu měďnatého /Xn/, roztok hydroxidu sodného (w = 0,10) /Xi (0,5-2)/.
Postup práce: * V kádince s 20 cm3 destilované vody zahřáté k varu rozpusťte 15 g pentahydrátu síranu měďnatého.
* K roztoku za neustálého míchání přidejte 50 cm3 roztoku NaOH (w = 0,10).
* Směs za neustálého míchání přiveďte k varu a zahřívejte ji, dokud se bude sraženina hydroxidu měďnatého rozkládat za vzniku příslušného oxidu.
* Vyloučený produkt promyjte vodou o objemu cca 100 cm3 destilované vody, oddělte filtrací za sníženého tlaku, znovu promyjte.
* Dostatečné promytí lze ověřit reakcí s roztokem Ba(NO3).
* K roztoku za neustálého míchání přidejte 50 cm3 roztoku NaOH (w = 0,10).
* Směs za neustálého míchání přiveďte k varu a zahřívejte ji, dokud se bude sraženina hydroxidu měďnatého rozkládat za vzniku příslušného oxidu.
* Vyloučený produkt promyjte vodou o objemu cca 100 cm3 destilované vody, oddělte filtrací za sníženého tlaku, znovu promyjte.
* Dostatečné promytí lze ověřit reakcí s roztokem Ba(NO3).
M(CuO) = 79,54 g/mol
m(CuO) = 5 g
M(NaOH) = 39,99 g/mol
?(NaOH, 10%) = 1,1089 g/cm3
m(NaOH) = ?
V(NaOH, 10%) = ?
2 NaOH + CuSO4• 5H2O ?› Cu(OH)2 + Na2SO4 + 5 H2O
Cu(OH)2 ?› CuO + H2O
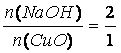
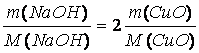
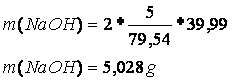
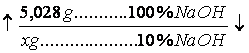
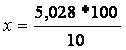
x = 50,3 g NaOH 10%
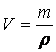
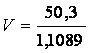
V = 45,34 ml NaOH 10%
m(CuO) = 5 g
M(NaOH) = 39,99 g/mol
?(NaOH, 10%) = 1,1089 g/cm3
m(NaOH) = ?
V(NaOH, 10%) = ?
2 NaOH + CuSO4• 5H2O ?› Cu(OH)2 + Na2SO4 + 5 H2O
Cu(OH)2 ?› CuO + H2O
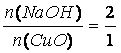
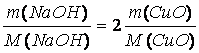
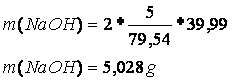
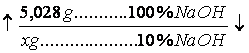
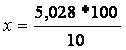
x = 50,3 g NaOH 10%
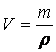
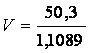
V = 45,34 ml NaOH 10%


